
腸管不全と小腸移植について
腸管不全とは?
腸管機能の低下により、生命の維持や成長に最低限必要な栄養、水分、電解質を腸管から吸収できず、経静脈的な補給を要する病態です。(※1)
経静脈的な補給により生存は可能ですが、慢性的な栄養障害、カテーテル感染症、敗血症、肝臓・腎臓等の臓器障害などを発症するリスクがあります。経静脈的補給を行うためのカテーテルを留置する血管の確保が難しくなると、静脈栄養が継続できなくなります。
※1:Pironi, L. et al. ESPEN endorsed recommendations. Definition and classification of intestinal failure in adults. Clin. Nutr. 34: 171–180, 2015.
対象疾患は?
対象疾患は主に以下の3つに分類されます。
- 短腸症候群
血流障害、外傷、腫瘍などによって小腸の大部分が外科的に切除された状態です。
(中腸軸捻転、腹壁破裂、外傷、壊死性腸炎、腸閉鎖、腫瘍、その他) - 腸管運動障害
小腸の壁にある筋肉を効果的に動かすことができないため、食べ物を効率よく運べない状態です。
(ヒルシュスプルング病、ヒルシュスプルング病類縁疾患、慢性特発性偽性腸閉塞(CIIP)、巨大膀胱短小腸結腸腸管蠕動不全症(MMIHS)、その他) - 消化・吸収障害
腸管が存在するにもかかわらず、水分や栄養素を十分に吸収できない状態です。
(クローン病、微絨毛封入体病、吸収不良症候群、難治性下痢、腸管リンパ管拡張症、蛋白漏出性胃腸症、その他)
腸管不全の症状は?
疾患や病態にもよりますが、以下が挙げられます。
- 経口摂取困難・食事が十分取れない
- 慢性的な腹部症状(腹痛、嘔吐、下痢、人工肛門排液が多い、腹部膨満など)
- 脱水症状
- 成長障害、栄養障害
- 精神的な負担・苦痛
- その他
腸管不全の合併症は?
腸管不全の合併症は、以下が挙げられます。
- 肝障害:腸管不全合併肝障害、胆石・胆嚢炎、脂肪肝、黄疸
- 感染:カテーテル関連血流感染症や消化管感染症など
- 中心静脈の狭窄・閉塞
- 腎障害
- 消化管出血:肝障害を伴う門脈圧亢進症に合併した食道胃静脈瘤出血、腸管うっ滞などに伴う消化管びらん・潰瘍など
- 心機能障害
- その他
腸管不全の重症度について
わが国では短腸症候群や腸管運動障害、消化・吸収不良障害を含む“小腸機能障害”は身体障害の一つとして認定され、静脈栄養依存度と残存腸管長、小腸機能の喪失範囲に応じて1~4等級に規定されます。
その他にも、中心静脈アクセスルートの減少(閉塞3箇所以上)、頻回なカテーテル感染、肝障害などの合併が腸管不全の予後に関与することが知られており、こうした病態を考慮した治療戦略が腸管リハビリテーションに求められます。
短腸症候群(SBS)
静脈栄養の依存度が最も重要な因子であり、さらに残存小腸の長さ、回盲弁や結腸の有無などによる詳細な重症度分類が提唱されます。
小児では年齢や体格を考慮した標準的な腸管長をもとに、その25%未満をSBSと定義しますが、具体的には小児慢性特定疾患の定義に成人の定義を加えた後述の定義および重症度分類が、日本小児外科学会、日本外科代謝栄養学会で承認されています。
<診断基準>
以下のA+Bの項目を満たし、Cの鑑別すべき疾患を除外したもの。
A 短小腸の基準
①小腸の75%以上を切除していること
②小腸の長さが、小児で75㎝未満、成人で1.5m未満であること、ただし乳幼児期は小腸の残存腸管が30cm未満であること
B 症状
中心静脈栄養への依存がある、慢性の腸管栄養吸収障害や水様性下痢を認める
C 鑑別診断
急性および一過性の栄養吸収障害や下痢(重症度Ⅰ~Ⅱ度に相当する)、炎症性腸疾患:クローン病、潰瘍性大腸炎
<重症度分類>
栄養吸収障害および水様性下痢により日常生活が著しく障害されており、重症度Ⅲ度以上のものを重症例とする。
重症度
Ⅰ度:急性期:腸管吸収機能不全に対し、中心静脈栄養を一過性に必要とする
Ⅱ度:適応期:腸管吸収機能不全が回復し、中心静脈栄養を離脱する見込みがある
Ⅲ度:慢性期:腸管吸収機能不全が遷延または悪化し、中心静脈栄養を離脱する見込みがない
Ⅲ-a:一部の栄養素あるいは水分の消化吸収機能障害を有するもの
Ⅲ-b:多数の栄養素および水分の消化管吸収機能障害を有するもの
腸管運動障害
指定難病に認定されている慢性特発性偽性腸閉塞(CIIP)、巨大膀胱短小腸結腸腸管蠕動不全症(MMIHS)、腸管神経節細胞僅少症においては、下記を満たすものが重症例として定義されます。
【腹部膨満、嘔気・嘔吐、腹痛などの腸閉塞症状により、日常生活が著しく障害されており、かつ以下の3項目のうち、少なくとも1項目以上を満たすもの】
1)静脈栄養を必要とする。
2)経腸栄養管理を必要とする。
3)継続的な消化管減圧を必要とする。
重症度と疫学について:これまでの研究報告より
厚生労働科研福澤班による全国調査 腸管不全354例(2006-2011年)
・悉皆調査ではないが、欧州で報告されている発生頻度5-20/100万と同程度で、本邦でも500-1000人程度の患者数が推定された。
・5年間の静脈栄養離脱率は35%、死亡率は12%であった。9%で重度肝障害を伴い、16%で3本以上の中心静脈が閉塞し、これらの因子が予後に相関した。
Pironiらによる在宅静脈栄養のレビュー
成人腸管不全の5年生存率は平均70%(58-83%)で、腸管リハビリテーションチームが関与しなければ死亡リスクは増加する。
Pediatric lntestinal Failure Consortiumの前向き観察研究
5年で小児腸管不全の約半数がenteral autonomy(腸管自立)を達成し、残りの半分は静脈栄養から離脱できず、約1/4に小腸移植が実施され、その1/4が死亡していた。
腸管不全と医療費助成
小児慢性特定疾病に対する医療費助成
厚生労働省により指定されている小児慢性特定疾病の患児を持つ家庭の医療費の負担を軽減するための制度です。
対象年齢
18才未満。ただし18歳到達時点において本事業の対象で、かつ18歳到達後も引き続き治療が必要と認められる場合には、20歳未満も対象です。
腸管不全における主な対象疾患
ヒルシュスプルング病、慢性特発性偽性腸閉塞症、腸管神経節細胞僅少症、巨大膀胱短小腸結腸腸管蠕動不全症、短腸症(短腸症候群)、クローン病
引用元:小児慢性特定疾病情報センターHP
難病医療費助成制度
厚生労働省により難病と指定されている病気の治療に関して、医療費の自己負担を軽減する制度です。
対象年齢
年齢制限無し
腸管不全における主な対象疾患
クローン病、ヒルシュスプルング病(全結腸型又は小腸型)、慢性特発性偽性腸閉塞症、腸管神経節細胞僅少症、巨大膀胱短小腸結腸腸管蠕動不全症
引用元:難病情報センターHP
腸管リハビリテーションプログラムとは
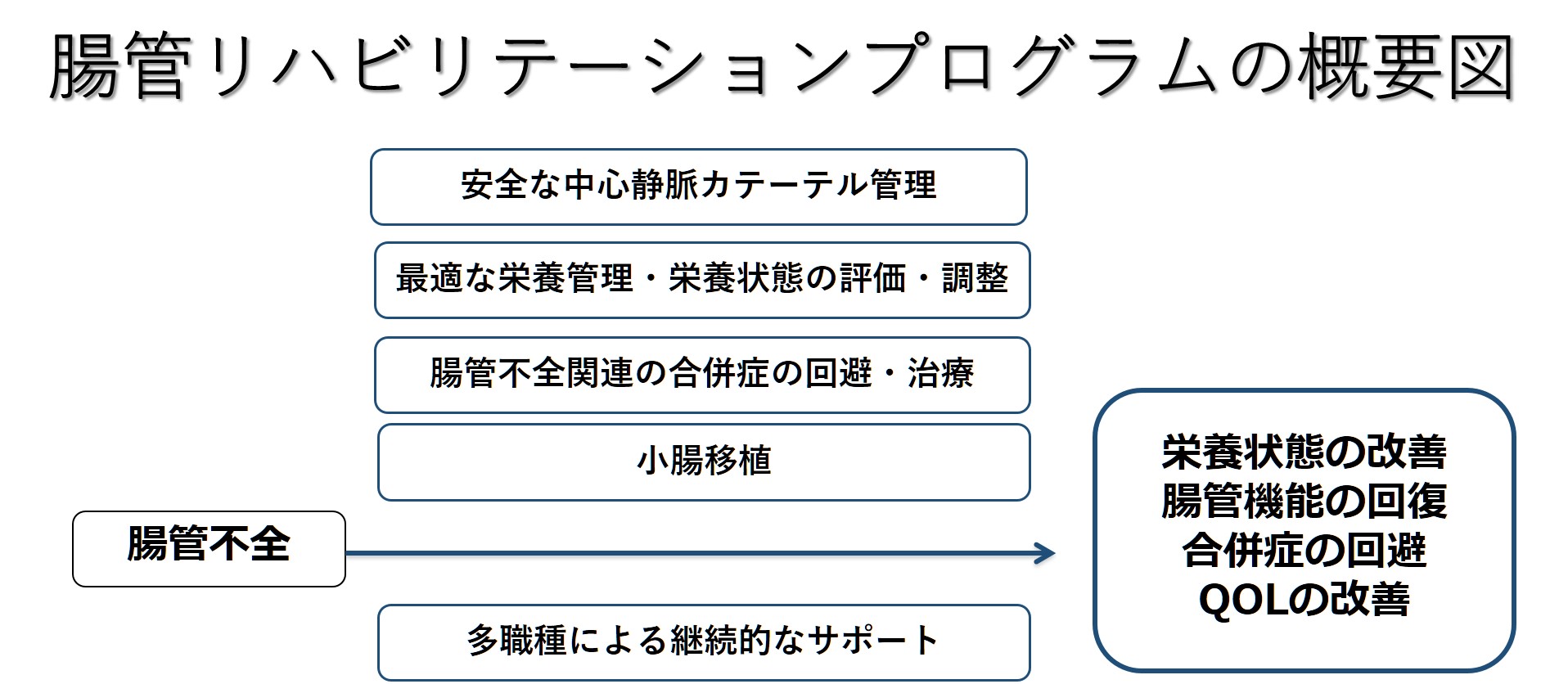
腸管不全治療の基本は、残存する腸管の機能を有効に活用することで静脈栄養の依存度を軽減し、様々な合併症の予防や治療に努めることです。
種々の内科的治療および移植を含む外科的治療だけでなく、精神的支援、疼痛管理、在宅移行などの社会的支援も含めた多職種による包括的支援・治療サポートを「腸管リハビリテーションプログラム」と呼びます。
状態が安定しない場合には、腸管リハビリテーションプログラムを有する医療機関に早期に相談することが推奨されます。
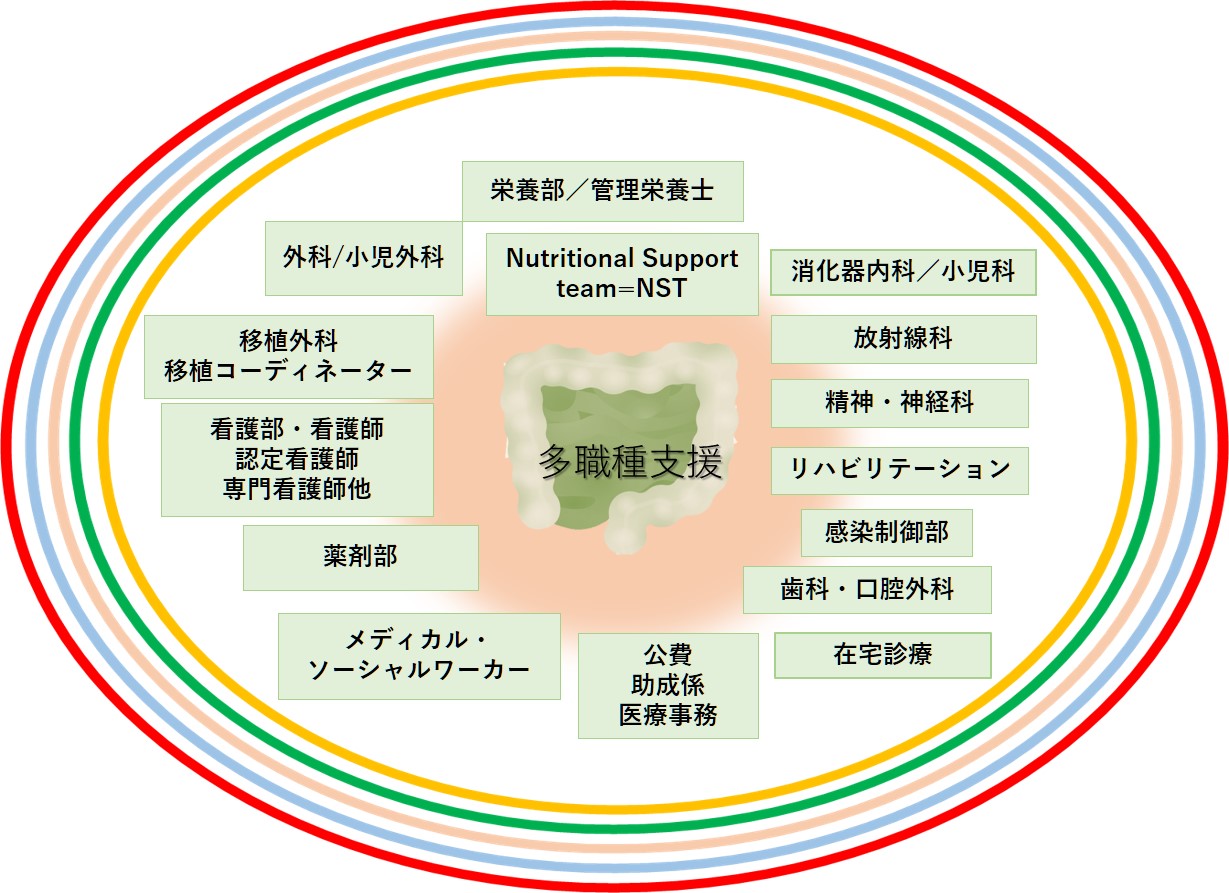
医師(消化器内科・消化器外科、移植外科、小児科、小児外科、心療内科、精神科、麻酔科、放射線科、リハビリテーション科など)、歯科医師だけでなく、看護師、栄養士、コーディネーター、ソーシャルワーカー、理学療法士などの多職種で構成し、その連携による多職種支援がQOLの改善・維持に重要です。
重症腸管不全患者の対応施設一覧
- 北海道大学病院
- 東北大学病院
- 慶応義塾大学病院
- 国立成育医療研究センター
- 埼玉県立小児医療センター
- 金沢医科大学病院
- 京都大学医学部附属病院
- 大阪大学医学部附属病院
- 九州大学病院
- 熊本大学病院
- 長崎大学病院
(日本移植学会ホームページ内臓器移植Q&Aより。2021年3月現在)
小腸移植とは?
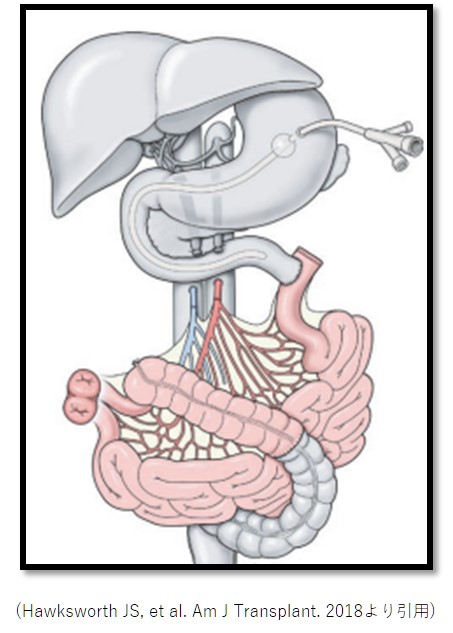
小腸移植とは、障害を受けた小腸或いは疾患のある小腸を摘出し、提供された健康な小腸に置き換えることです。移植が成功すると中心静脈栄養が不要となり、食事制限や水分制限もなくなることが期待されます。十分に機能した小腸によって今よりも健康な状態を手に入れることが可能になります。
小腸移植には、脳死体ドナーからと生体ドナーからの二種類の移植があり、これまでに全世界で約5,500人の患者に対して行われています。そのほとんどは脳死体ドナーより提供を受けています。
本邦では2023年12月までに41名に45回の小腸移植が施行されています。うち、生体小腸移植は13例、脳死小腸移植は32例行われています。小腸移植術後にはタクロリムスとステロイドを中心とする多剤併用免疫抑制療法が必要となります。
参照元:一般社団法人 日本移植学会 ファクトブック2024
小腸移植の適応について

小腸移植は、肝障害の重症度やカテーテル敗血症の頻度、残存する中心静脈アクセスルートの本数などにより、具体的な小腸移植の適応基準が提唱されていますが、実際にその適応と時期を判断するのは困難なことが多く、QOLを含めた総合的な判断が必要です。
一方、合併症を繰り返すうちに敗血症で死亡する症例、中心静脈アクセスルートの枯渇、重篤な肝腎障害により、移植の機会と時期を失う例も少なくありません。
海外では2015年にブエノスアイレスで行われた国際小腸移植シンポジウムで移植適応の見直しが議論され、ワーキンググループによる新たな適応基準が2020年に提唱され、小児においては表25-11が該当します。
小腸移植後は?
小腸移植の成績は1年生存率9割近く、5年生存率が約7割です。中長期的にはさらなる改善が必要で、その要因としては以下に挙げる拒絶反応、感染症などが挙げられます。
移植後は人工肛門が造設されます。拒絶反応の診断のために内視鏡検査を行う必要があるからです。中心静脈カテーテルは移植後早期は使用しますが、移植腸管が十分に機能し、栄養・水分量の観点などに問題ないと判断されれば離脱・抜去が可能になります。
2023年12月の国内のデータでは、生存患者の全員が部分的に経静脈栄養から離脱し、約80%が経静脈栄養から完全に離脱していました。
拒絶反応
臓器移植後合併症のうち、拒絶反応は最も大きな問題です。小腸は他の移植と比べても拒絶反応を起こしやすく、移植後3か月以内に約50〜70%に急性拒絶反応が起こるといわれています。いったん拒絶が生じると進行が早く、移植した小腸から容易に血流感染症を発症し致命的となります。移植後、数年経過してから急性拒絶反応を発症することもあります。
発症時には、人工肛門からの排液量の増加や 色調の悪化が生じ、人工肛門から内視鏡検査を行い診断を確定します。慢性拒絶反応も、移植腸管喪失の大きな要因の一つです。
感染症/腎機能障害
感染症
小腸移植後に特異的な腸炎やカテーテル敗血症には注意が必要です。サイトメガロウイルスやEBウイルス感染症、ニューモシスチス肺炎の頻度も高いとされています。
PTLD(移植後リンパ増殖性疾患)および GVHD(移植片対宿主病)も発生頻度が高い致命的な合併症です。
腎機能障害
移植前からの脱水傾向などを背景に、移植後はカルシニューリン阻害剤の高用量投与、抗菌薬・抗真菌薬の長期投与、多量の人工肛門排液による脱水などにより腎障害が増悪する傾向にあります。
